Саксенда — отзывы
Отзыв:
Небольшая предыстория… мне 29 лет, рост 164, вес неделю назад был 102,5 кг., размер одежды 54-56-58 (грудь большая)… У меня инсулинорезистентность с времен шагания под стол. Все детство бегали по врачам и слышали только одно «ДИЕТЫ ДИЕТЫ ДИЕТЫ!!!!!», пока, однажды, в 19 лет не попала к толковому врачу, которая и выявила данный недуг + СПКЯ (на тот момент я всила примерно 90 кг). С горем пополам, за 3 года мой организм, как говорится, поставили на ноги. Путем лечения гормонами и Метформином дошла до отметки 60 кг. с этого момента я полностью отказалась от сахара, всегда была активной и питалась правильно, за исключением дней «разгрузок» (крупные праздники). Но к несчастью позитивная картина наблюдалась недолго. Через года 2 — 2,5 после серьезного стресса организм послал меня нафиг и все стало возвращаться на круги своя. (при том, что я по-прежнему придерживалась 1200-1500 кКал и без сахара и мучного). Это получается к 26 годам я опять вернулась к исходной точке. Вес дико рос, причем за месяц могла прибавить от 2х до 5 кг. Приняла решение опять обратиться в врачу, ног к несчастью врач, которая меня наблюдала ушла на пенсию. Связь с ней была утеряна. Я горевала… Далее был период «денег на ветер». Сменила несколько врачей, куча анализов. Ответ один — ДИЕТАААААА!!!! Начала понимать что приближается депрессия. Приняла решения самостоятельно повторить ранее пройденный курс лечения. Эффект — 1 кг в месяц.
Некоторое время спустя все бросила. Муж требовал чтобы я заканчивала с самоедством и дала себе в конце концов отдохнуть морально. (спасибо ему за это). И вот, пол года спустя, изучив кучу отзывов и рекомендаций знакомых решилась сходить в очередной раз к врачу. О чем я не пожалела. Она — единственная, кому стало интересно «а почему так то?», кому было не безразлично, что я страдаю. Просидев на приеме около часа, врач изучала абсолютно всю историю моей болезни, я ей притаранила все что у меня могло оставаться на руках, что я смогла сохранить от исследований, и мы совместно приняли решение — надо дать толчок. медлить нельзя. Тем более, если я хочу в будущем стать мамой. И вот, врач приняла решение, что целесообразно будет начать применять Саксенду. Скажу честно, долго решалась брать или нет (дорого, побочки, последствия все эти мысли не давали покоя). Врач уверила, что ее назначают даже детям с 12 лет, но строго под наблюдением и индивидуальной дозировкой. А ведь это очень серьезный препарат. Причем относительно «молодой» в медицине. Ломалась-ломалась, в итоге решилась. Врач прописала колоть в комплексе с приемом Глюкофаж Лонг 1000. Прошла ровно неделя Колю дозировку 0,6 + половинку глюкофажа, все перед сном. Что за неделю успела приметить. Отеков стало меньше в ногах, ушло 4 кг. веса, периодическое «помутнение» с подташнивание бывает. Свежий воздух + мятная жвачка помогают быстро вернуться в струю. Подавляет аппетит. Мое питание: утро — кофе, бутерброд с сыром; обед — бульон или творог; ужин — мясо (куриная грудка, говядина) на пару, пара огурчиков свежих. Все это запихиваю в себя. Переживаю, что желудок не отблагодарит. ну и конечно водичка. Стараюсь попивать постоянно, да и на самом деле хочется пить почти всегда))))) Сколько пью — не замеряла. Но больше обычного.
Еще хотелось бы вот что добавить от себя. ДЕВОЧКИ!!!! Саксенда — лекарственный препарат, не БАД. Он должен появиться в вашей аптечке только (!) по назначению врача. Если вы весите 55 — 65 кг., и хотите от этого препарата чудного действия — триста раз подумайте, а не навредит ли он вам?!
Саксенда раствор для подкожн введен заполненые шприц-ручки 6мг/мл 3мл N 5
Действующие вещества
Лираглутид
Состав
В 1 мл препарата содержится: действующее вещество: лираглутид 6 мг (в одной предварительно заполненной шприц-ручке содержится 3 мл раствора, что соответствует 18 мг лираглутида); вспомогательные вещества: натрия гидрофосфата дигидрат 1,42 мг, фенол 5,5 мг, пропиленгликоль 14,0 мг; кислота хлористоводородная/натрия гидроксид (для коррекции pH), вода для инъекций до 1 мл.
Механизм действия
Действующее вещество препарата Саксенда® — лираглутид — представляет собой аналог человеческого глюкагоноподобного пептида-1 (ГПП-1), произведённый методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae, имеющий 97% гомологичности аминокислотной последовательности эндогенному человеческому ГПП-1.
Лираглутид связывается и активирует рецептор ГПП-1 (ГПП-1Р). Лираглутид устойчив к метаболическому распаду, период его полувыведения из плазмы после подкожного введения составляет 13 ч. Фармакокинетический профиль лираглутида, позволяющий вводить его пациентам 1 раз в сутки, является результатом самоассоциации, в результате которой происходит замедленное всасывание препарата; связывания с белками плазмы; а также устойчивости к дипептидилпептидазе-4 (ДПП-4) и нейтральной эндопептидазе (НЭП). ГПП-1 является физиологическим регулятором аппетита и потребления пищи. ГПП-1Р обнаружены в нескольких областях головного мозга, задействованных в регулировании аппетита. В исследованиях на животных введение лираглутида приводило к его захвату в специфических областях головного мозга, включая гипоталамус, где лираглутид посредством специфической активации ГПП-1Р усиливал сигналы о насыщении и ослаблял сигналы о голоде, тем самым приводя к уменьшению массы тела.
Лираглутид уменьшает массу тела у человека преимущественно посредством уменьшения массы жировой ткани. Уменьшение массы тела происходит за счёт уменьшения потребления пищи. Лираглутид не увеличивает 24-часовой расход энергии. Лираглутид регулирует аппетит с помощью усиления чувства наполнения желудка и насыщения, одновременно ослабляя чувство голода и уменьшая предполагаемое потребление пищи. Лираглутид стимулирует секрецию инсулина и уменьшает неоправданно высокую секрецию глюкагона глюкозозависимым образом, а также улучшает функцию бета-клеток поджелудочной железы, что приводит к снижению концентрации глюкозы натощак и после приёма пищи. Механизм снижения концентрации глюкозы также включает небольшую задержку опорожнения желудка.
Показания Препарат Саксенда® показан в качестве дополнения к низкокалорийной диете и усиленной физической нагрузке для длительного применения с целью коррекции массы тела у взрослых пациентов с ИМТ: — ≥30 кг/м2 (ожирение) или — ≥ 27 кг/м2 до < 30 кг/м (избыточная масса тела) при наличии хотя бы одного связанного с избыточной массой тела сопутствующего заболевания, такого как нарушение толерантности к глюкозе, сахарный диабет 2 типа, артериальная гипертензия, дислипидемия или синдром обструктивного апноэ во сне.
Противопоказания
- повышенная чувствительность к лираглутиду или любому из вспомогательных компонентов препарата;
- медуллярный рак щитовидной железы в анамнезе, в том числе в семейном;
- множественная эндокринная неоплазия 2 типа;
- тяжёлая депрессия, суицидальные мысли или поведение, в том числе в анамнезе.
Противопоказано применение у следующих групп пациентов и при следующих состояниях/заболеваниях в связи с отсутствием данных по эффективности и безопасности:
- нарушение функции почек тяжёлой степени;
- нарушение функции печени тяжёлой степени;
- детский возраст до 18 лет;
- период беременности и грудного вскармливания;
- сердечная недостаточность III-IV функционального класса (в соответствии с классификацией NYHA (Нью-Йоркская кардиологическая ассоциация));
- одновременное применение других препаратов для коррекции массы тела;
- одновременное применение с инсулином;
- вторичное ожирение на фоне эндокринологических заболеваний или расстройств пищевого поведения, или на фоне применения лекарственных препаратов, которые могут привести к увеличению массы тела.
Перед применением требуется консультация специалиста.Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач.Режим хранения, взаимодействие и побочные действия указаны в инструкции.
Неуклонный рост числа больных сахарным диабетом 2-го типа (СД2), особенно значимый в последние годы, заставляет постоянно пересматривать прогнозы [1]. Многие причины этой эпидемии к настоящему времени хорошо изучены. Показано, что старение населения приводит к закономерному росту заболеваемости СД2. Проведенные исследования свидетельствуют о том, что имеются возрастные механизмы повышения уровня глюкозы в плазме, особенно после еды. Считается, что каждые 10 лет после 50-летнего возраста содержание глюкозы натощак незначительно повышается, а постпрандиальная концентрация увеличивается на 0,5 ммоль/л [2]. В связи с этим старение населения можно отнести к некорригируемому фактору риска возникновения СД, особенно в экономически развитых странах. Однако гораздо больший удельный вес в патогенезе СД2 имеет избыток массы тела. Ожирение распространено как среди пожилых, так и среди людей среднего возраста, составляющих 40% населения [3]. Именно ожирение, развивающееся, как правило, после 35—40 лет и носящее название андроидного, висцеро-абдоминального ожирения, является основой развития метаболического синдрома — синдрома инсулинорезистентности [4]. Вместе с тем снижение чувствительности тканей к инсулину — не единственный фактор, приводящий к развитию СД2. Без нарушения секреторной способности β-клеток и уменьшения их количества СД2 не манифестирует. Хронологически первым звеном развития СД2 является свойственная больным висцеро-абдоминальным ожирением инсулинорезистентность. В случае сохранной секреторной способности β-клеток избыточная секреция инсулина какое-то время компенсирует инсулинорезистентность и позволяет в течение довольно длительного периода (до 10 лет) поддерживать нормогликемию. С течением времени наблюдается постепенное истощение секреторной способности β-клеток, а также значительное уменьшение их количества. Гипергликемия и дислипидемия, свойственные этому периоду заболевания, усугубляют дисфункцию β-клеток, значительно затрудняя лечение таких больных. Необходимо учитывать, что за счет длительной предшествующей гиперинсулинемии большинство больных ожирением к моменту постановки диагноза СД уже имеют целый ряд сердечно-сосудистых заболеваний, в частности, артериальную гипертензию и различные клинические проявления атеросклероза коронарных, мозговых и периферических артерий. Поэтому для замедления прогрессирования этих заболеваний при развитии СД следует как можно быстрее устранить гипергликемию.
В то же время интенсивный контроль гликемии сопряжен с риском гипогликемических состояний, чрезвычайно опасных у больных с высоким сердечно-сосудистым риском. Учитывая тот факт, что у более половины больных СД2 имеются сердечно-сосудистые заболевания или множественные факторы их риска, разработанные Российской ассоциацией эндокринологов алгоритмы лечения больных СД2 (2011) в качестве препаратов первого ряда, как для старта, так и для интенсификации терапии, рекомендуют средства, обладающие минимальной способностью индуцировать гипогликемии [5].
К этим препаратам относятся производные бигуанидов, ингибиторы дипептидил-пептидазы-4 (ДПП-4) и агонисты глюкагоноподобного пептида-1 (ГПП-1). Если производные бигуанидов относятся к хорошо проверенным средствам, то ингибиторы ДПП-4 и агонисты ГПП-1 являются новым классом препаратов инкретинового ряда и опыт их применения в клинической практике невелик. Эти препараты обладают уникальным действием инкретинов, которые регулируют гомеостаз глюкозы в глюкозозависимом режиме [6], положительно влияя на все этапы биосинтеза и секреции инсулина, а также препятствуя истощению пула инсулина в секреторных гранулах. Эндогенный инкретин, ГПП-1, обеспечивает до 70% постпрандиальной секреции инсулина β-клетками, одновременно подавляя продукцию глюкагона α-клетками островков Лангерганса [7]. При снижении уровня глюкозы в крови до 4,5 ммоль/л стимулирующее влияние ГПП-1 на инсулиновый ответ прекращается, а при гипогликемии ГПП-1 начинает стимулировать деятельность α-клеток поджелудочной железы. В результате повышается уровень глюкагона, усиливается физиологическая продукция глюкозы печенью, что способствует восстановлению нормального уровня гликемии. Таким образом, риск развития гипогликемии на фоне инкретиновой терапии практически отсутствует. Кроме того, как показано в экспериментальных исследованиях, что ГПП-1 стимулирует пролиферацию β-клеток и подавляет их апоптоз [8]. Инкретины обладают и дополнительными сахарснижающими эффектами, способствуя утилизации глюкозы жировыми и мышечными клетками и подавляя продукцию глюкозы печенью. Иными словами, они снижают инсулинорезистентность.
Терапия инкретинами не вызывает увеличения массы тела, не оказывает отрицательного влияния на артериальное давление (АД) и показатели липидного спектра крови [9]. Согласно рекомендуемым алгоритмам лечения больных СД2 (2011), в качестве препаратов первого ряда в дебюте заболевания при наличии ожирения и артериальной гипертензии предпочтительны агонисты ГПП-1, эффективно снижающие массу тела и систолическое АД.
В последние годы выявлен целый ряд плейотропных эффектов инкретинов, опосредованных G-белками. Рецепторы ГПП-1 имеются не только в поджелудочной железе, но и в клетках кишечника, желудка, почек, сердца, легких, а также в клетках периферической и центральной нервной системы. Стимуляция рецепторов ГПП-1 в подвздошной кишке приводит к усилению вагусного эффекта, снижению моторики желудочно-кишечного тракта, замедлению опорожнения желудка. Вероятно, этот эффект объясняет более быстрое насыщение и способствует снижению аппетита [10]. В ядрах гипоталамуса, регулирующих пищевое поведение, также обнаружены рецепторы ГПП-1, стимуляция которых также приводит к снижению аппетита и массы тела [11]. Введение агонистов ГПП-1 животным с сердечной недостаточностью повышает сердечный выброс, а при наличии ишемии миокарда — уменьшает площадь инфаркта [12].
Чрезвычайно важными представляются данные о существовании метаболита ГПП-1, способного стимулировать NO-зависимую вазодилатацию коронарных артерий, что позволяет предположить наличие у ГПП-1 кардиопротективного эффекта [13].
Влияние ГПП-1 на почки связано с усилением натрийуреза и диуреза предположительно за счет его прямого влияния на Na+/H+-транспорт в проксимальных канальцах почек. Кроме того, инкретины, не оказывая прямого влияния на клубочковую фильтрацию у здоровых людей, снижают гиперфильтрацию у инсулинрезистентных пациентов с повышенной массой тела [14]. Имеются экспериментальные данные о влиянии ГПП-1 на костную ткань. Предполагается, что их протективное действие осуществляется, по-видимому, через кальциотонинзависимые механизмы.
У больных СД2 и даже у лиц с преддиабетом инкретиновые эффекты снижаются, что нарушает выделение инсулина в ответ на прием углеводов [15]. Для коррекции этих нарушений предложено использовать две группы препаратов: ингибиторы ДПП-4 и аналоги ГПП-1. Применение препаратов, блокирующих фермент ДПП-4 (ситаглиптин, вилдаглиптин, саксаглиптин), приводит к поддержанию физиологического уровня ГПП-1 и увеличению периода полураспада эндогенного ГПП-1. Однако у больных СД2 чувствительность к ГПП-1 значительно снижена и для восстановления его эффектов требуется концентрация ГПП-1, в несколько раз превышающая физиологическую, что и объясняет отсутствие значимого сахарснижающего эффекта при лечении ингибиторами ДПП-4 у ряда больных. В то же время использование агонистов ГПП-1, не подверженных действию ДПП-4, представляется весьма перспективным.
Одним из таких препаратов является аналог человеческого ГПП-1 длительного действия — лираглутид (Виктоза), зарегистрированный в России в мае 2010 г. В отличие от других препаратов этого ряда, применяемых сегодня в клинической практике, Виктоза обладает высоким сродством к рецепторам эндогенного человеческого ГПП-1 и устойчива к протеолитической деградации ДПП-4. Период полужизни препарата достигает 13 ч, а длительность действия — до 24 ч, это позволяет вводить препарат всего один раз в день [16].
В данной работе представлен опыт применения препарата Виктоза в лечении пациентов с СД2.
Препарат назначался как в условиях стационара, так и амбулаторно. Основными показаниями для назначения препарата Виктоза были: подтвержденный СД2, отсутствие контроля гликемии на фоне приема средних или максимальных терапевтических доз одного или двух пероральных сахарснижающих препаратов (ПССП), а также наличие ожирения или избыточной массы тела. Обязательным условием назначения препарата Виктоза было сохранение функциональной активности β-клеток, подтвержденное нормальным или повышенным уровнем С-пептида. У большинства пациентов имелись сопутствующая патология сердечно-сосудистой системы, артериальная гипертензия и атерогенная дислипидемия. В связи с этим практически все наблюдаемые больные получали антигипертензивные, гиполипидемические препараты и дезагреганты, поэтому оценить дополнительные плейотропные эффекты аналога ГПП-1 было весьма сложно. Полипрагмазия, свойственная лечению больных СД2, как правило, вызвана стремлением достичь не только контроля гликемии, но и целевых уровней АД, липидного профиля крови, а также необходимостью лечения сопутствующих заболеваний (табл. 1).
Тем не менее при исходном обследовании перед назначением препарата Виктоза практически у всех пациентов большинство показателей контроля превышали целевые значения. Группу наблюдения составили пациенты с исходным уровнем гликированного гемоглобина (HbA1с) выше 8%.
При назначении препарата Виктоза неукоснительно соблюдалась инструкция по использованию этого лекарственного средства. Так, ни один из пациентов не получал инсулин, не были использованы нерациональные комбинации ПССП (например, ингибиторы ДПП-4 и агонист ГПП-1). Среди пациентов не было лиц, страдающих онкологическими заболеваниями, органическими заболеваниями центральной нервной системы, тяжелой сердечной, легочной, почечной или печеночной недостаточностью.
Препарат Виктоза назначался подкожно в начальной дозе 0,6 мг один раз в день в одно и то же время независимо от приема пищи с последующим увеличением дозы до 1,2 мг/сут.
Представлены данные 6-месячного лечения 71 больного СД2, среди которых было 45 мужчин и 26 женщин; средний возраст составил 51,1±5,2 года при длительности заболевания 6,4±4,2 года. В большинстве случаев это были больные с выраженным ожирением (средний ИМТ составил 35,8±2,3 кг/м2). У всех пациентов отмечался плохой контроль гликемии. Уровень HbA1с составлял в среднем 8,9±1,2%. До начала терапии препаратом Виктоза 14 больных получали монотерапию препаратами сульфонилмочевины (ПСМ), 17 — монотерапию метформином, 23 — комбинированную терапию двумя ПССП (ПСМ + метформин) и 19 — не получали медикаментозную терапию по поводу СД.
В анализируемой группе все показатели гликемии были достаточно высокими: глюкоза в плазме натощак — 9,8±0,8 ммоль/л, постпрандиальная гликемия — 12,1±1,8 ммоль/л. У большинства пациентов была артериальная гипертензия (42 человека, 59%), у всех обследованных была выявлена атерогенная дислипидемия.
Результаты лечения препаратом Виктоза оценивались через 3 и 6 мес после начала его применения (табл. 2).
Уже через 3 мес уровень HbA1с практически достиг целевого уровня. Через 6 мес лечения препаратом Виктоза уровень HbA1с нормализовался и составил 6,6%. Концентрация глюкозы в плазме натощак и постпрандиальная гликемия через 6 мес также достигли целевых значений. При этом ни у одного пациента в течение 6 мес не отмечено ни одного случая тяжелой гипогликемии. Легкие гипогликемические состояния наблюдались редко у пациентов, получавших препарат Виктоза в комбинации с другими ПССП: у 8 из 31 больного, получавшего препарат Виктоза в сочетании с ПСМ. У пациентов, исходно не получавших сахарснижающих препаратов, уровень HbA1с достиг целевых значений уже через 3 мес лечения и составил 6,9±1,1%, а через 6 мес — 6,5±0,9%.
Представленные данные подтверждают, что препарат Виктоза обладает выраженной гипогликемизирующей способностью, сопоставимой с таковой наиболее активных неинсулиновых препаратов, используемых в лечении СД2. Через полгода применения препарата Виктоза у пациентов с СД2 и плохим контролем гликемии, в том числе на фоне предшествующей терапии ПССП, удалось достичь идеального контроля в отсутствие выраженных гипогликемических состояний.
Следует подчеркнуть, что назначение препарата Виктоза привело не только к значительному улучшению гликемического контроля у всех представленных пациентов; у пациентов, ранее получавших терапию ПССП и не достигших оптимального контроля, добавление Виктоза позволило снизить дозу ПССП (у 11 из 14 пациентов, находящихся на терапии ПСМ, и у 11 из 23 пациентов, ранее получавших ПСМ в сочетании с метформином) или полностью отменить секретогоги (у 3 больных, ранее получавших ПСМ, и у 9 — ранее получавших ПСМ + метформин).
Чрезвычайно важным представляется снижение массы тела у всех больных, получавших препарат Виктоза. Снижение веса составило от 1,3 до 16,5 кг. В среднем через 3 мес после начала лечения масса тела снижалась на 5,1 кг, а через 6 мес — на 6,4 кг. Наибольшее снижение массы тела наблюдалось у пациентов с исходно более выраженной степенью ожирения. Так, в группе пациентов с ИМТ 30—35 кг/м2 снижение массы тела через 3 мес составило 3,3 кг, через 6 мес — 3,9 кг. В группе больных с ИМТ 35—40 кг/м2 масса тела снизилась на 4,6 и 5,9 кг через 3 и 6 мес соответственно. У пациентов с морбидным ожирением (ИМТ выше 40 кг/м2) наблюдалось самое выраженное похудание: на 7,6 кг через 3 мес и на 10,1 кг за полгода. Какой-либо связи между динамикой снижения уровня гликемии и HbA1с и ИМТ выявить не удалось. Следует отметить, что все пациенты соблюдали умеренно ограничительную диету (1700—1800 ккал в сутки), но на фоне лечения препаратом Виктоза им удавалось гораздо легче, чем ранее, соблюдать рекомендации по питанию. Вместе с тем динамика массы тела не зависела от наличия и выраженности диспепсических явлений.
Кроме перечисленных клинических эффектов, терапия препаратом Виктоза у пациентов с СД2 сопровождалась достоверным снижением уровня холестерина и триглицеридов в сыворотке. Общий холестерин снизился за 6 мес с 6,7 до 5,1 ммоль/л, а уровень триглицеридов — с 2,3 до 1,5 ммоль/л. Следует отметить, что большинство пациентов по показаниям получали те или иные гиполипидемические препараты (статины или фибраты), однако их дозы были стабильными в течение всего периода наблюдения. Уменьшение выраженности дислипидемии можно объяснить, с одной стороны, улучшением контроля гликемии и снижением массы тела, с другой — уменьшением дозировки ПСМ.
Из 71 пациента с СД2 52 получали постоянную гипотензивную терапию, включающую ингибиторы АПФ или блокаторы рецепторов ангиотензина II, а 29 больным дополнительно были назначены блокаторы кальциевых каналов. Коррекция гипотензивной терапии проводилась до включения больных в исследование. За время наблюдения ни у одного из пациентов не отмечалось гипертонических кризов или значимых повышений АД. В течение всего наблюдения у большинства пациентов удалось поддерживать целевые значения АД; отчасти этому способствовала достаточно высокая комплаентность больных. Вместе с тем не исключено и собственное гипотензивное влияние препарата Виктоза, так как известно натрийуретическое действие инкретинов. У 9 больных потребовалось снизить дозу гипотензивных препаратов из-за тенденции к гипотонии, что, возможно, было связано со снижением массы тела.
Терапия препаратом Виктоза хорошо переносилась. Никто из больных не предъявлял жалобы на тошноту или иные диспепсические расстройства. Наиболее частыми ощущениями на фоне начала применения препарата Виктоза были чувство более быстрого, чем раньше, насыщения обычным количеством пищи. При этом аппетит и удовольствие от приема пищи были сохранены. Двое больных отметили склонность к запорам в начале терапии; регулярный стул восстановился в течение следующих 3—4 дней. Применение слабительных средств не требовалось ни в одном случае.
Таким образом, проведенное исследование показало, что у пациентов с СД2 Виктоза является весьма эффективным и безопасным препаратом как для достижения хорошего контроля гликемии, так и в плане контроля диабета в целом. Неоспоримыми дополнительными преимуществами терапии препаратом Виктоза являются возможность эффективно снижать избыточную массу тела, улучшать профиль АД и показатели липидного спектра крови. Полученные данные позволяют рекомендовать более широкое использование препарата Виктоза как в виде монотерапии на ранних этапах заболевания, так и в комплексном лечении СД2.
Чем нас лечат: Саксенда
Но вот в возможности предотвратить диабет второго типа у таких препаратов ученые сомневаются. Влияние лираглутида на риск развития инсулинонезависимого диабета доказать пока не удалось, несмотря на ряд исследований, в которых он понижает содержание в крови некоторых веществ-предвестников болезни. Долгосрочные эффекты препарата на артериальное давление у пациентов с ожирением тоже почти не изучены.
Indicator.Ru рекомендует: принимать под наблюдением врача
Препарат отпускается по рецепту, поэтому самолечение вряд ли будет проблемой. И правильно: при повышенной дозировке можно снизить уровень сахара в крови до опасных значений (это называется гипогликемия), заполучив в награду обмороки или что похуже. Да и рисков из-за неправильного введения инъекций никто не отменял. Большинству же пациентов вряд ли грозит что-то серьезное: самые частые побочные эффекты, которые возникают примерно у 5% пациентов, будут не опасны, а, скорее, неприятны, как тошнота или запор.
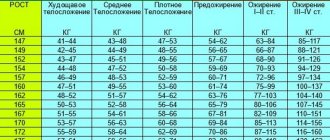
Препарат рекомендуют пациентам с индексом массы тела выше 30 (или выше 27, но с осложнениями). Принимать его ради желания сбросить пару кило от своих 60, да еще и без диабета второго типа будет опасно, а вот, например, если ваша масса тела равна 90 кг при росте 165 см, такие показатели уже могут считаться оправданными. Лекарство действительно будет эффективным и поможет сбросить около 6% массы тела, что больше, чем у ряда других препаратов для похудения.
Есть подозрения, что препарат повышает риск рака щитовидной и поджелудочной железы, а также панкреатита и проблем с сердцем, но они пока лишь косвенно подтверждены. Если такая опасность и существует, то возникает она нечасто.
А вот кому лучше не использовать Саксенду, так это пациентам с нарушением работы почек и печени, панкреатитом, болезнями желчного пузыря, а также (не до конца доказанный эффект, но лучше поостеречься) людям с суицидальными наклонностями. Не рекомендуют его пациентам с учащенным сердцебиением в состоянии покоя. При беременности и грудном вскармливании безопасность для ребенка не доказана, поэтому лучше не рисковать.
Сочетание препарата с другими лекарствами от диабета должно быть очень продуманным: действие одних он может многократно усилить, другим будет мешать, поэтому посоветуйтесь с врачом. Варфарин и другие производные кумарина нужно применять с осторожностью.
Кроме того, не стоит забывать о здоровом образе жизни: препарат может стать хорошим дополнением к питанию с дефицитом калорий и физической активности, но без них результаты вас вряд ли впечатлят.
Наши рекомендации нельзя приравнивать к назначению врача. Перед тем, как начать принимать тот или иной препарат, обязательно посоветуйтесь со специалистом.
Понравился материал? Добавьте Indicator.Ru в «Мои источники» Яндекс.Новостей и читайте нас чаще.
Подписывайтесь на Indicator.Ru в соцсетях: Facebook, ВКонтакте, Twitter, Telegram, Одноклассники.